گاز هگزا فلوراید گوگرد و تاریخچه آن:
هگزا فلوراید گوگرد یا SF6 از ترکیب یک اتم گوگرد با شش اتم فلوراید تشکیل شده است. این گاز برای نخستین بار در سال ۱۹۰۰ در لابراتوار داروسازی در پاریس کشف شد.
در سال ۱۹۳۷، شرکت جنرال الکترونیک برای اولین بار گاز هگزا فلورید گوگرد را به صورت کاربردی مورد استفاده قرار داد، به عنوان مثال از گاز هگزا فلوراید گوگرد به عنوان ماده عایق استفاده شد.
بعد از جنگ جهانی دوم، در اواسط قرن بیستم، محبوبیت استفاده از گاز هگزا فلوراید گوگرد همانند ماده ای عایق در سیستم الکترونیکی به سرعت افزایش یافت.
شرکت مواد شیمیایی آلید و پینسالت نخستین شرکت صنعتی آمریکایی بودند که در سال ۱۹۴۸ این گاز را به صورت تجاری تولید کردند. در طول سال ۱۹۶۰، استفاده از گاز هگزا فلوراید گوگرد در کلید ابزار ولتاژ بالا محبوبیت پیدا کرد. همان طور که تقاضا برای این گاز افزایش یافت، بسیاری از تولیدکنندگان در اروپا و آمریکا در این دوره شروع به تولید گاز هگزا فلوراید گوگرد در مقیاس زیاد کردند.
در آغاز، گاز هگزا فلوراید گوگرد تنها با هدف عایق سازی در سیستم الکترونیکی استفاده میشد، اما خیلی زود کشف شد که این گاز خاصیت خاموش کننده خارق العادهای برای جرقه یا قوس الکترونیکی دارد. همچنین این گاز در مدارشکن به عنوان ابزار خاموش کننده قوس الکترونیکی مورد استفاده قرار گرفت. نخستین گاز هگزا فلوراید گوگرد در پاریس در سال ۱۹۶۶ به عنوان عایق فرعی استفاده شد. مدارشکنهای ولتاژ هگزا فلوراید گوگرد در سال ۱۹۷۱ وارد بازار شدند.
تولید گاز هگزا فلوراید گوگرد
SF6 یا ملکولهای گاز هگزا فلوراید گوگرد به طور تجاری با استفاده از واکنش فلوئور ( حاصل از الکترولیز ) با گوگرد بدست میآید.
در طی فرآیند تولید این گاز، محصولات دیگری مانند SF4, SF2, S2F2 وS2F10 نیز با درصد کم تولید میشوند. نه تنها این محصولات جانبی، بلکه ناخالصی مانند هوا، رطوبت، دی اکسید کربن نیز در این گاز در مرحله تولید وجود دارد. تمام این محصولات جانبی و ناخالصیها در مراحل مختلف تصفیه فیلتر شده و محصول نهایی به صورت خالص و تسویه شده بدست میآید.
ویژگیهای شیمیایی هگزا فلوراید گوگرد
برای بررسی ویژگیهای شیمیایی گاز هگزا فلوراید گوگرد، ابتدا ساختار این ملکول را معرفی میکنیم، یک ملکول گوگرد با شش اتم فلوئور احاطه شده است. عدد اتمی گوگرد ۱۶ است. به این معنا که دو الکترون در سطح انرژی اول، ۸ الکترون در سطح انرژی دوم و ۶ الکترون باقیمانده هم در سطح انرژی سوم قرار دارند. پیکربندی الکترون از اتم گوگرد به صورت ۲،۸،۶ است، ۱S2 2S2 2P6 3S2 3P4.
اتم فلوئور دارای عدد اتمی ۹ است. پیکربندی الکترون آن به صورت ۱S2 2S2 2P5 است.
هر اتم گوگرد در ملکول SF6 پیوند کووالانسی با ۶ اتم فلوئور دارد. در این روش اتم گوگرد دارای ۶ پیوند کووالانسی است، یعنی ۶ جفت الکترون در هر لایه خارجی دارد و هر اتم فلوئور هم ۸ الکترون در بیرونیترین لایهشان دارند.
در اینجا میتوان مشاهده کرد که در لایه خارجی اتم هگزا فلوراید گوگرد ۱۲ الکترون به جای ۸ الکترون وجود دارد. یعنی در اینجا گوگرد از قانون کلی هشت هشتی ساختار اتمی پیروی نکرده است، در این قانون اتم پایدار به ۸ الکترون در خارجیترین لایه نیاز دارد. این مورد هم استثناء نیست. بعضی از عناصر در دوره سوم و پایین میتوانند پیوندی را ایجاد کنند و فراتر از ۸ الکترون در لایه خارجیشان داشته باشند.
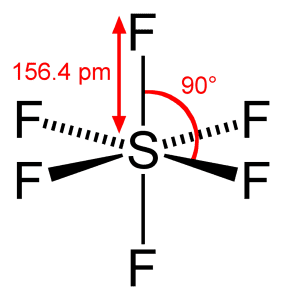
ساختار مولکولی این گاز در زیر نشان داده شده است. در این روش، هگزا فلوراید گوگرد به طور کامل از شرایط ساختاری پایدار بهره برده است. شعاع کارآمد ملکول هگزا فلوراید گوگرد برابر با ۲٫۳۸۵ A است. این پیکربندی استثنایی الکترونی و ساختار این گاز هگزا فلوراید گوگرد را به شدت پایدار کرده است. این گاز میتواند بدون تجزیه در ساختار ملکولی در دمای بالای ۵۰۰ درجه سانتیگراد ثابت باشد. این گاز به شدت غیرقابل اشتعال است. ملکول H2O و Cl نمیتوانند با این گاز واکنش نشان دهند. همچنین با اسید هم واکنش نشان نمیدهد.
گاز هگزا فلوراید گوگرد یکی از سنگینترین گازهاست. چگالی این گاز در دمای ۲۰ درجه سانتیگراد در فشار یک اتمسفر برابر با ۶٫۱۳۹ کیلوگرم بر مترمکعب است که ۵ برابر بالاتر از هوا در شرایط مشابه است. وزن ملکولی این گاز برابر با ۱۴۶٫۰۶ است.
تغییرات فشار با دما برای هگزا فلوراید گوگرد به صورت خطی است و در محدوده درجه حرارت -۲۵ تا +۵۰ درجه بسیار کم است.
گرمای ویژه حجمی این گاز بسیار بالاست. در حدود ۳٫۷ برابر بیشتر از هواست، به همین دلیل این گاز در تجهیزات الکترونیکی تأثیر خنکسازی فوقالعادهای دارند.
هدایت حرارتی این گاز بسیار بالا نیست، حتی کمتر از هواست. با این حال برای اثر خنکسازی مدارشکن کاملاً مناسب است. زیرا در طول تفکیک ملکول هگزا فلوراید گوگرد در اطراف قوس الکترونیکی، این ملکول مقدار زیادی گرما را جذب میکند و سپس زمانی این گرما آزاد میشود که ملکول در مجاورت قوس الکترونیکی بازسازی میشود. این فرآیند به انتقال بسیار سریع گرما از فصل گرم به فصل سرد کمک خواهد کرد. به همین دلیل، این گاز دارای تأثیرات خنکسازی عالی در دمای بالاست، اگر چه هدایت حرارتی هگزا فلوراید گوگرد چندان بالا نیست.
خواص الکترونیکی گاز هگزا فلوراید گوگرد
گاز هگزا فلوراید گوگرد تا حد زیادی خاصیت الکترونگاتیوی دارد. به خاطر خاصیت الکترونگاتیوی بالای آن، الکترونهای آزادی را جذب میکند که به خاطر قوس بین تماسها با قطع کننده مدار تولید میشوند. ترکیب الکترونهای آزاد با این ملکولها منجر به تولید یونهای بزرگ و سنگین میشود، که قابلیت حرکت بسیار پایینی دارند. به خاطر جذب الکترونهای آزاد و حرکت کم یونها، هگزا فلوراید گوگرد ویژگی دی الکتریک بسیار عالی دارد. قدرت دی الکتریک گاز هگزا فلوراید گوگرد حدود ۲٫۵ برابر بیشتر از هواست.
فهرست ویژگیهای گاز هگزا فلوراید گوگرد
چگالی در دمای ۲۰ درجه سانتیگراد: ۶٫۱۴ kg/m3
رنگ گاز: بیرنگ
وزن ملکولی: ۱۴۶٫۰۶
هدایت حرارتی: ۰٫۰۱۳۶ w/mK
دمای بحرانی: ۴۵٫۵۵°C
چگالی بحرانی: ۷۳۰ Kg/m3
فشار بحرانی: ۳٫۷۸ MPa
سرعت صوت در گاز هگزا فلوراید گوگرد: ۱۳۶ m/s. این سرعت ۳ برابر کمتر از هواست.
ضریب شکست: ۱٫۰۰۰۷۸۳
تشکیل حرارتی: -۱۲۲۱٫۶۶ Kg/mol
گرمای ویژه: ۹۶٫۶ j/mole K
فیلد تفکیک مربوط به فشار: ۸۹ V/m Pa
ثابت دی الکتریک نسبی در ۲۵درجه سانتیگراد و ۱ نوار مطلق: ۱٫۰۰۲۰۴
عامل اتلاف یا tanδ در ۲۵ درجه سانتیگراد و ۱ نوار مطلق: <2 × ۱۰-۷
سؤالات عینی در سیستم قدرت الکترونیکی(MCQs)
























